مجاني (1) 30 مل من الماء البكتيري
مع أوامر مؤهلة أكثر500 دولار أمريكي.
(يستبعد منتجات الكبسولة ، والببتيدات التجميلية ، ورموز الترويجي والشحن)
ما هو LL-37 (CAP-18)؟
LL-37 هيكل

LL-37 Research
LL-37 والأمراض الالتهابية
LL-37 ، على الرغم من وصفها في المقام الأول على أنها ببتيد مضاد للميكروبات ، في الواقع ، يلعب دورًا في عدد من الأمراض الالتهابية مثل الصدفية والذئبة والتهاب المفاصل الروماتويدي وتصلب الشرايين. اعتمادًا على البيئة الالتهابية المحلية والخلايا المعنية المعنية ، تحتوي LL-37 على العديد من السلوكيات التي تعدل الجهاز المناعي المختلفة. تم العثور على:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- زيادة إنتاج IL-18 ، و
- انخفاض مستويات لويحات تصلب الشرايين[1].
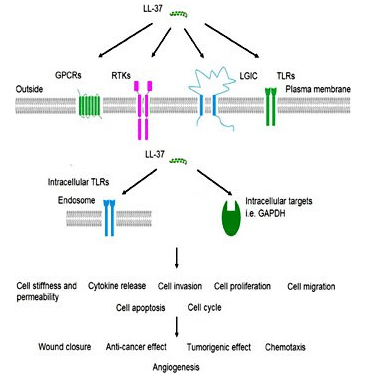
LL-37 هو مضادات الميكروبات القوية
LL-37 هو جزء من الجهاز المناعي الفطري ، وبالتالي يعد أحد الأجزاء الأولى من الجهاز المناعي الذي يتم تنشيطه أثناء العدوى. تشير الأبحاث في التهابات الجلد إلى أن الجلد الطبيعي له مستويات منخفضة جدًا من LL-37 ولكن الببتيد يتراكم بسرعة في وجود مسببات الأمراض الغازية. وقد تبين أن الببتيد يعمل جنبا إلى جنب مع البروتينات الأخرى ، مثل بيتا ديفنسسين البشري 2 لمكافحة العدوى[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 ومرض الرئة
LPS ، كما ذكر أعلاه ، ليست فريدة من نوعها لجدران الخلايا البكتيرية. تم العثور عليها في عدد من الكائنات الحية المختلفة ، وفي بعض الحالات ، تصبح محمولة جواً عندما تكون البيئة ملوثة بالعفن أو الفطريات الأخرى. عندما يتم استنشاق LPS ، يستجيب أنسجة الرئة الطبيعية عن طريق الإنتاج. لسوء الحظ ، تكون الاستجابة غير كافية في كثير من الأحيان لمنع متلازمة الغبار السامة والتسبب في أمراض الجهاز التنفسي مثل الربو ، مرض الانسداد الرئوي المزمن ، وأكثر من ذلك. البحث في استخدام LL-37 كعلاج مستنشق لمتلازمة الغبار السام قيد التنفيذ حاليًا[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].فهم LL-37 في التهاب المفاصل
تشير الأبحاث في الفئران إلى أن LL-37 موجود في تركيزات عالية في المفاصل المتأثرة بالتهاب المفاصل الروماتويدي. على وجه الخصوص ، يبدو أن الببتيد مرتبط بالأحداث المرضية لالتهاب المفاصل. ومع ذلك ، ليس من الواضح إذا كان الببتيد سببًا أو تنظيمه في هذه المفاصل هو جزء من محاولة الجسم للتحكم في العملية المرضية[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. بناءً على هذه الدراسة ، من المعقول التكهن بأن LL-37 ربما يكون له نشاط وقائي في التهاب المفاصل ، مما قد يفسر تركيزاته العالية في الأنسجة مع التهاب كبير. يتم دعم هذه التكهنات من خلال حقيقة أن LL-37 ومشتقاتها تبين أنها تنظم الالتهاب الناجم عن إنترلوكين 32 ، وهو جزيء ارتبط مباشرة بشدة التهاب المفاصل الالتهابية[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. لقد تبين أن LL-37 يرتبط بـ TLR4 ويعزز التأثيرات المؤيدة للالتهابات أو المضادة للالتهابات. ما يفعله في إعداد التنظيم TLR3 غير واضح ، لكن البحث مستمر. فكرة أنه قد يقلل من الالتهاب بشكل انتقائي ليس من غير المعقول بالنظر إلى أنه تم العثور على LL-37 لتقليل استجابات البلاعم المؤيدة للالتهابات بشكل انتقائي في الماضي[13].LL-37 والأمعاء
تشير الأبحاث في ثقافات الخلايا إلى أن LL-37 له العديد من الآثار في الأمعاء. أولاً ، يزيد الببتيد من ترحيل الخلايا اللازمة للحفاظ على الحاجز الظهاري للأمعاء. ثانياً ، يقلل LL-37 من موت الخلايا المبرمج في وضع الالتهاب المعوي ، مما يساعد على إبطاء التسبب في عدد من الحالات الالتهابية. بشكل عام ، يشير البحث إلى أن LL-37 قد يكون علاجًا مساعد مفيدًا في ظروف الأمعاء الالتهابية ، بعد جراحة الأمعاء ، أو في وضع الالتهابات المعوية الحادة. قد يثبت أنه مفيد كمساعد للعلاج بالمضادات الحيوية ، مما يساعد على منع الآثار الجانبية للجيش الاستثماري التي تحد في كثير من الأحيان استخدام المضادات الحيوية عن طريق الفم[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. حاليا ، مثبطات TNF-alpha هي الدعامة الأساسية للعلاج لظروف الأمعاء الالتهابية. فهي أدوية فعالة ، ولكن لها عدد من الآثار الجانبية الخطيرة بما في ذلك التسبب في زيادة جذرية في خطر الإصابة بالخطيرة ، مثل مرض السل. يمكن أن يساعد تطور علاجات LL-37 لمرض الأمعاء الالتهابية في تقليل الاعتماد على مثبطات TNF-alpha وتحسين المراضة والوفيات في هذا السكان المريض.LL-37 وسرطان الأمعاء
أنتجت الأبحاث المتعلقة بـ LL-37 والسرطان نتائج مختلطة ، ولكن يبدو أن الببتيد مفيد في وضع سرطانات الأمعاء والمعدة ، بما في ذلك سرطان الخلايا الحرشفية الفموية المرتبطة بالتدخين واستخدام التبغ. ومن المثير للاهتمام ، يبدو أن هذه الآثار تتوسط فيها مسار تعتمد على فيتامين-د ، والذي قد يفسر سبب ارتباط الفيتامين سابقًا بانخفاض خطر الإصابة بسرطان الجهاز الهضمي. يبدو أن فيتامين (د) يحث على نشاط مضاد للسرطان من الضامة المرتبطة بالورم عبر LL-37[16].LL-37 ونمو الأوعية الدموية
يبدو أن LL-37 تؤدي إلى توليف البروستاجلاندين E2 (PGE2) في الخلايا البطانية. يرتبط PGE2 بكل من الألم الالتهابي ومع نمو الأوعية الدموية ، ولكن هذه الآثار تختلف بناءً على المكان الذي يتم فيه التعبير عن الجزيء. في الخلايا البطانية ، يؤدي PGE2 إلى تطور الأوعية الدموية في عملية تسمى الأوعية الدموية[17]. يمكن أن يكون هذا جيدًا وسيئًا ، اعتمادًا على الإعداد المعين. كانت القدرة على تنظيم تكوين الأوعية الدموية محور الكثير من الأبحاث في العقود القليلة الماضية لأنها تؤثر على تطور السرطان ، وأمراض القلب ، ونتائج السكتة الدماغية ، وشفاء الجروح ، وأكثر من ذلك. يوفر نشاط LL-37 وسيلة مفيدة لاستكشاف مسار تكوين الأوعية بالإضافة إلى نموذج للتدخلات المستقبلية المحتملة لتعزيز نمو الأوعية الدموية عند الحاجة (مثل أمراض القلب) وتثبيطه عندما يكون ضارًا (مثل السرطان).بحث LL-37 المستمر
كاتب المقال
مؤلف المجلة العلمية
الاقتباسات المرجعية
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.