Eau bactériostatique libre (1) 30 ml
avec des commandes qualifiées sur500 USD.
(exclut les produits de capsule, les peptides cosmétiques, les codes promotionnels et l'expédition)
Qu'est-ce que LL-37 (CAP-18)?
Structure LL-37

Recherche LL-37
LL-37 et maladies inflammatoires
Le LL-37, bien que principalement présenté comme un peptide antimicrobien, joue en fait un rôle dans un certain nombre de maladies inflammatoires telles que le psoriasis, le lupus, la polyarthrite rhumatoïde et l'athérosclérose. Selon l'environnement inflammatoire local et les cellules particulières impliquées, LL-37 a plusieurs comportements de modulation du système immunitaire différents. Il a été trouvé à:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- augmenter la production d'IL-18, et
- diminuer les niveaux des plaques athérosclérotiques[1].
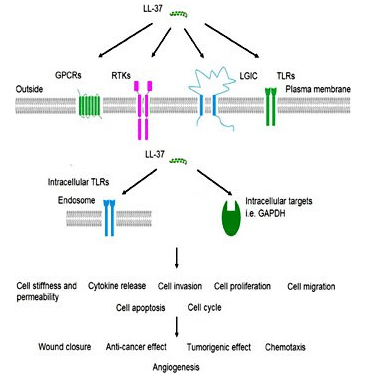
LL-37 est un puissant antimicrobien
LL-37 fait partie du système immunitaire inné et, en tant que tel, est l'un des premiers morceaux du système immunitaire à être activés pendant l'infection. La recherche sur les infections cutanées suggère que la peau normale a des niveaux très faibles de LL-37 mais que le peptide s'accumule rapidement en présence d'agents pathogènes envahisseurs. Il a été démontré que le peptide fonctionne en tandem avec d'autres protéines, comme la bêta-défensine humaine 2 pour lutter contre l'infection[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 et maladie pulmonaire
Le LPS, comme mentionné ci-dessus, n'est pas unique aux parois cellulaires bactériennes. Il se trouve dans un certain nombre d'organismes différents et, dans certains cas, devient en l'air lorsqu'un environnement est contaminé par la moisissure ou d'autres champignons. Lorsque le LPS est inhalé, le tissu pulmonaire normal répond en produisant. Malheureusement, la réponse est souvent inadéquate pour prévenir le syndrome de la poussière toxique et la pathogenèse des maladies respiratoires comme l'asthme, la MPOC, etc. La recherche sur l'utilisation de LL-37 comme traitement inhalé du syndrome de la poussière toxique est actuellement en cours[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Comprendre LL-37 dans l'arthrite
La recherche chez le rat indique que le LL-37 se trouve dans des concentrations élevées dans les articulations affectées par la polyarthrite rhumatoïde. En particulier, le peptide semble être associé aux événements pathologiques de l'arthrite. Il n'est pas clair, cependant, si le peptide est causal ou sa régulation à la hausse de ces articulations fait partie de la tentative du corps de contrôler le processus pathologique[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Sur la base de cette étude, il est raisonnable de spéculer que LL-37 a probablement une activité protectrice dans l'arthrite, ce qui pourrait expliquer ses concentrations élevées dans les tissus avec une inflammation substantielle. Cette spéculation est soutenue par le fait que LL-37 et ses dérivés se sont avérés réguler l'inflammation causée par l'interleukine-32, une molécule qui a été directement associée à la gravité de l'arthrite inflammatoire[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. Il a été démontré que le LL-37 se lie à TLR4 et favorise les effets pro-inflammatoires ou anti-inflammatoires. Ce qu'il fait dans le cadre de la régulation positive TLR3 n'est pas claire, mais la recherche est en cours. L'idée que cela pourrait réduire de manière sélective l'inflammation n'est pas déraisonnable étant donné que le LL-37 s'est avéré réduire sélectivement les réponses des macrophages pro-inflammatoires dans le passé[13].LL-37 et l'intestin
La recherche dans les cultures cellulaires indique que LL-37 a plusieurs effets dans l'intestin. Premièrement, le peptide augmente la migration des cellules nécessaires pour maintenir la barrière épithéliale de l'intestin. Deuxièmement, LL-37 réduit l'apoptose dans le cadre de l'inflammation intestinale, contribuant à ralentir la pathogenèse d'un certain nombre de conditions inflammatoires. Dans l'ensemble, la recherche indique que le LL-37 peut être un traitement adjuvant utile dans des conditions d'intestin inflammatoires, après une chirurgie intestinale ou dans le cadre d'infections intestinales aiguës. Il peut même s'avérer utile comme adjuvant à l'antibiothérapie, aidant à prévenir les effets secondaires gastro-intestinaux qui limitent souvent l'utilisation d'antibiotiques oraux[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Actuellement, les inhibiteurs du TNF-alpha sont un pilier du traitement des conditions intestinales inflammatoires. Ce sont des médicaments efficaces, mais ont un certain nombre d'effets secondaires graves, notamment une augmentation drastique du risque d'infection grave, comme la tuberculose. Le développement de traitements basés sur LL-37 de la maladie inflammatoire de l'intestin pourrait aider à réduire la dépendance à l'égard des inhibiteurs du TNF-alpha et à améliorer la morbidité et la mortalité dans cette population de patients.LL-37 et cancer intestinal
La recherche concernant le LL-37 et le cancer a produit des résultats mitigés, mais le peptide semble être bénéfique dans le cadre des cancers intestinaux et gastriques, y compris le carcinome épidermoïde oral associé au tabagisme et à l'usage du tabac. Fait intéressant, ces effets semblent être médiés par une voie dépendante de la vitamine-D, ce qui peut expliquer pourquoi la prise de la vitamine a déjà été associée à un risque réduit de cancer gastro-intestinal. Il semble que la vitamine D induit l'activité anticancéreuse des macrophages associés à la tumeur via LL-37[16].LL-37 et croissance des vaisseaux sanguins
LL-37 semble déclencher la synthèse de la prostaglandine E2 (PGE2) dans les cellules endothéliales. Le PGE2 est associé à la fois à des douleurs inflammatoires et à la croissance des vaisseaux sanguins, mais ces effets diffèrent en fonction de l'endroit où la molécule est exprimée. Dans les cellules endothéliales, PGE2 déclenche le développement des vaisseaux sanguins dans un processus appelé angiogenèse[17]. Cela peut être à la fois bon et mauvais, selon le cadre particulier. La capacité de réguler l'angiogenèse a été au centre de nombreuses recherches au cours des dernières décennies car elle a un impact sur le développement du cancer, les maladies cardiaques, les résultats des accidents vasculaires cérébraux, la cicatrisation des plaies, etc. L'activité LL-37 offre un moyen utile pour sonder la voie de l'angiogenèse ainsi qu'un modèle d'interventions futures potentielles pour favoriser la croissance des vaisseaux sanguins en cas de besoin (par exemple, les maladies cardiaques) et la découragent lorsqu'elle est préjudiciable (par exemple le cancer).Recherche en cours LL-37
Article auteur
Auteur de journal scientifique
Citations référencées
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.