Acqua batteriostatica libera (1) da 30 ml
con ordini qualificati$ 500 USD.
(Esclude prodotti capsule, peptidi cosmetici, codici promozionali e spedizione)
Cos'è LL-37 (CAP-18)?
Struttura LL-37

Ricerca LL-37
LL-37 e malattie infiammatorie
LL-37, sebbene fatturato principalmente come peptide antimicrobico, svolge in realtà un ruolo in una serie di malattie infiammatorie come la psoriasi, il lupus, l'artrite reumatoide e l'aterosclerosi. A seconda dell'ambiente infiammatorio locale e delle cellule particolari coinvolte, LL-37 ha diversi comportamenti modulanti del sistema immunitario. È stato scoperto per:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- aumentare la produzione di IL-18 e
- diminuire i livelli di placche aterosclerotiche[1].
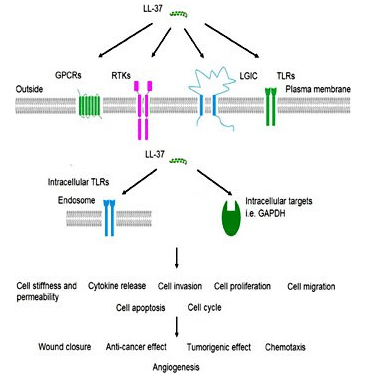
LL-37 è un potente antimicrobico
LL-37 fa parte del sistema immunitario innato e come tale è uno dei primi pezzi del sistema immunitario ad essere attivato durante l'infezione. La ricerca sulle infezioni della pelle suggerisce che la pelle normale ha livelli molto bassi di LL-37 ma che il peptide si accumula rapidamente in presenza di agenti patogeni invasori. È stato dimostrato che il peptide funziona in tandem con altre proteine, come la beta-difensina 2 umana per combattere l'infezione[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 e malattia polmonare
LPS, come menzionato sopra, non è unico per le pareti cellulari batteriche. Si trova in diversi organismi e, in alcuni casi, diventa disperso nell'aria quando un ambiente è contaminato da muffa o altri funghi. Quando l'LPS viene inalato, il normale tessuto polmonare risponde producendo. Sfortunatamente, la risposta è spesso inadeguata per prevenire la sindrome della polvere tossica e la patogenesi delle malattie respiratorie come l'asma, la BPCO e altro ancora. È attualmente in corso ricerche sull'uso di LL-37 come trattamento per inalazione per la sindrome della polvere tossica[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Comprensione di LL-37 nell'artrite
La ricerca sui ratti indica che LL-37 si trova in alte concentrazioni nelle articolazioni colpite dall'artrite reumatoide. In particolare, il peptide sembra essere associato agli eventi patologici dell'artrite. Non è chiaro, tuttavia, se il peptide è causale o la sua up-regolazione in queste articolazioni è una parte del tentativo del corpo di controllare il processo patologico[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Sulla base di questo studio, è ragionevole ipotizzare che LL-37 abbia probabilmente attività protettiva nell'artrite, che potrebbe spiegare le sue alte concentrazioni nei tessuti con infiammazione sostanziale. Questa speculazione è supportata dal fatto che LL-37 e i suoi derivati hanno dimostrato di regolare l'infiammazione causata dall'interleuchina-32, una molecola che è stata direttamente associata alla gravità dell'artrite infiammatoria[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. È stato dimostrato che LL-37 si lega a TLR4 e promuove effetti pro-infiammatori o antinfiammatori. Che fa nel contesto dell'up-regolazione di TLR3 non è chiaro, ma la ricerca è in corso. L'idea che potrebbe ridurre selettivamente l'infiammazione non è irragionevole dato che è stato riscontrato che LL-37 riduce selettivamente le risposte dei macrofagi pro-infiammatori in passato[13].LL-37 e l'intestino
La ricerca nelle colture cellulari indica che LL-37 ha diversi effetti nell'intestino. Innanzitutto, il peptide aumenta la migrazione delle cellule necessarie per mantenere la barriera epiteliale dell'intestino. In secondo luogo, LL-37 riduce l'apoptosi nell'impostazione dell'infiammazione intestinale, contribuendo a rallentare la patogenesi di una serie di condizioni infiammatorie. Nel complesso, la ricerca indica che LL-37 può essere un utile trattamento adiuvante in condizioni intestinali infiammatorie, a seguito di chirurgia intestinale o in ambito di infezioni intestinali acute. Può anche rivelarsi utile come adiuvante alla terapia antibiotica, contribuendo a prevenire gli effetti collaterali GI che spesso limitano l'uso di antibiotici orali[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Attualmente, gli inibitori del TNF-alfa sono un pilastro di trattamento per le condizioni intestinali infiammatorie. Sono farmaci efficaci, ma hanno una serie di gravi effetti collaterali, tra cui causando un drastico aumento del rischio di gravi infezioni, come la tubercolosi. Lo sviluppo di trattamenti basati su LL-37 di malattia infiammatoria intestinale potrebbero aiutare a ridurre la dipendenza dagli inibitori del TNF-alfa e migliorare la morbilità e la mortalità in questa popolazione di pazienti.LL-37 e cancro intestinale
La ricerca su LL-37 e il cancro ha prodotto risultati contrastanti, ma il peptide sembra essere utile nell'impostazione di tumori intestinali e gastrici, inclusi carcinoma a cellule squamose orali associate al fumo e all'uso del tabacco. È interessante notare che questi effetti sembrano essere mediati da un percorso dipendente dalla vitamina-D, il che può spiegare perché l'assunzione della vitamina è stata precedentemente associata a un rischio ridotto di cancro GI. Sembra che la vitamina D induca l'attività anticancro dei macrofagi associati al tumore tramite LL-37[16].LL-37 e crescita dei vasi sanguigni
LL-37 sembra innescare la sintesi della prostaglandina E2 (PGE2) nelle cellule endoteliali. PGE2 è associato sia al dolore infiammatorio che alla crescita dei vasi sanguigni, ma questi effetti differiscono in base al punto in cui la molecola viene espressa. Nelle cellule endoteliali, PGE2 innesca lo sviluppo dei vasi sanguigni in un processo chiamato angiogenesi[17]. Questo può essere sia buono che cattivo, a seconda della particolare impostazione. La capacità di regolare l'angiogenesi è stata al centro di molte ricerche negli ultimi decenni perché influisce sullo sviluppo del cancro, le malattie cardiache, i risultati dell'ictus, la guarigione delle ferite e altro ancora. L'attività di LL-37 offre un mezzo utile per sondare la via dell'angiogenesi, nonché un modello per potenziali interventi futuri per promuovere la crescita dei vasi sanguigni quando necessario (ad esempio malattie cardiache) e scoraggiarlo quando è dannoso (ad esempio il cancro).Ricerca LL-37 in corso
Autore dell'articolo
Autore della rivista scientifica
Citazioni di riferimento
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.