


카테고리 :펩티드 완성 된 제품, 펩타이드와 그들의 복용량
유리 (1) 30 ml 세균성 물
자격을 갖춘 주문이 있습니다$ 500 USD.
(캡슐 제품, 미용 펩티드, 프로모션 코드 및 배송 제외)
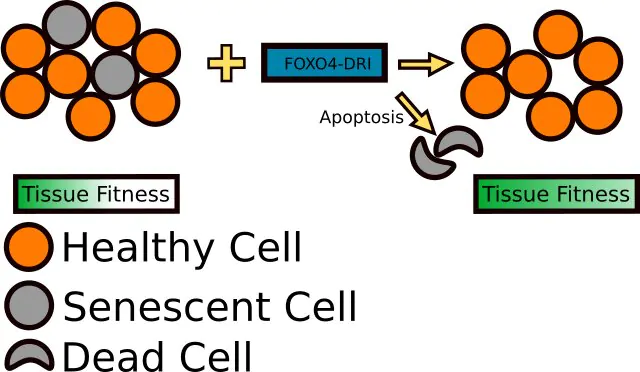
FOXO4와 노화의 관계는 복잡하고 여전히 완전히 이해되지 않았습니다. 그러나 단백질이 그 영향을 미치는 메커니즘을 설명하는 데 도움이되는 좋은 증거가 있습니다. 잘 연구 된 선충에 대한 연구C. elegansFOXO4는 인슐린 유사 성장 인자 수용체 신호 전달 및 따라서 세포 수명 제어, 스트레스 저항 및 유전자 조절에 영향을 미친다는 것을 보여줍니다.[3]. 또한 FOXO4는 p53 단백질과 상호 작용하여 세포 사이클을 조절하는 것으로 보인다.
천연 FOXO4는 실제로 세포주기의 조절 인자 인 p53을 격리하고 아 pop 토 시스를 유도 할 수 없음으로써 노화 세포를 보호합니다. FOXO4-DRI는 정상적인 FOXO4/p53 메커니즘을 방해하고 후자의 단백질을 노화 세포에서 아 pop 토 시스를 유도합니다. 결과는 조직 항상성의 노화 관련 연관 손실의 개선이된다.[4], [5]. 과학자들은 이것을 노화 세포의 치료 적 제거에 의해 활력으로 언급한다. 과정이 과일 나무를 가지 치기와 다르지는 않습니다. 죽은 손상된 가지와 손상된 가지 (노화 세포)를 제거함으로써 에너지는 나무의 더 건강한 부분으로 리디렉션되어 과일 생산 및 성장으로 리디렉션됩니다. 이 동일한 과정은 전반적인 건강에 해로운 기능에 기여하는 세포가 제거 될 때 장기 및 조직 수준에서 발생하여 자원이 건강한 세포에 중점을 둘 수 있습니다.
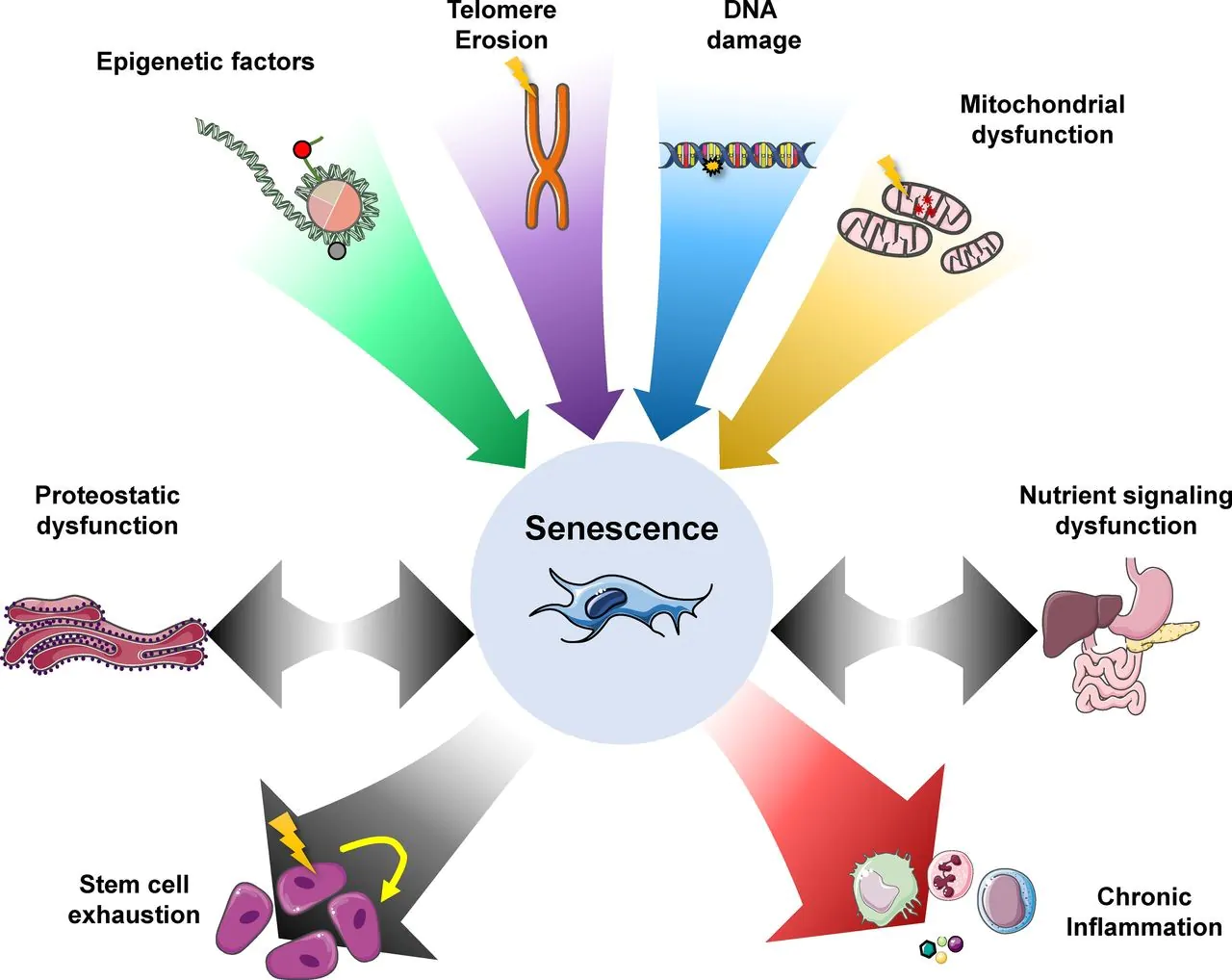 원천:세포 생물학 저널
원천:세포 생물학 저널
이 이미지는 노화에 어떤 요인이 어떤 요인과 노화 결과가 무엇인지 표시합니다. 노화 세포를 제거하면 줄기 세포 소진이 완화되지는 않지만 속도가 느려질 수 있습니다. 그러나 그것은 심장 질환, 뇌졸중 등과 같은 여러 상태의 잘 확립 된 동인 인 만성 염증을 줄이는 데 도움이됩니다.
신체가 고칠 수있는 능력을 넘어서는 세포 손상은 건강 범위에 대한 주요 제한 중 하나입니다. 유기체가 건강하고 최적으로 기능하는 시간 인 건강 범위는 일반적으로 수명보다 짧습니다. HealthSpan의 감소는 노화로 나타납니다. 건강 범위를 연장하는 능력은 더 많은 수년간 살아남을 수는 없지만 건강이 더 커지고 더 나은 기능을하면서 우리에게 할당 된 년을 살아갈 수 있습니다. 마우스 모델에서 FOXO4는 노화 된 마우스의 건강 범위를 개선하여 체력, 모피 밀도 및 신장 기능이 증가하는 것으로 나타났습니다. 마우스는 반드시 더 오래 살 필요는 없지만 건강, 심지어 나이가 더 많아서 장애가 적고 심장병, 근골격계 기능 장애 등과 같은 연령 관련 상태가 줄어 듭니다.[2].
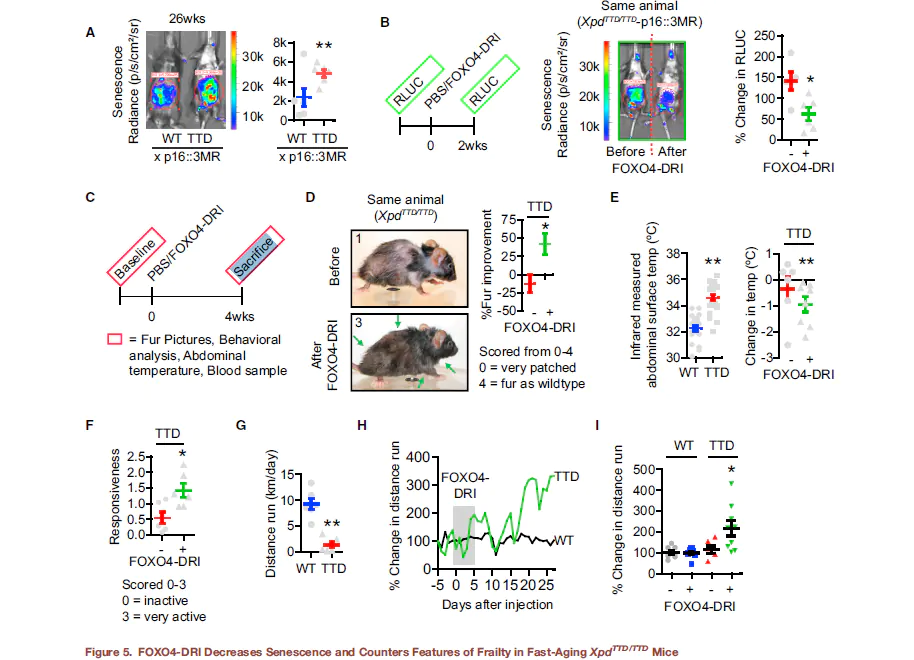 모피 밀도에 의해 지시 된 바와 같이, 개선 된 체력을 나타내는 이미지는 노화를 모델링하는 데 사용 된 화학 주성 물질에 적용한 후 FOXO4-DRI로 처리 된 마우스에서 :
모피 밀도에 의해 지시 된 바와 같이, 개선 된 체력을 나타내는 이미지는 노화를 모델링하는 데 사용 된 화학 주성 물질에 적용한 후 FOXO4-DRI로 처리 된 마우스에서 :
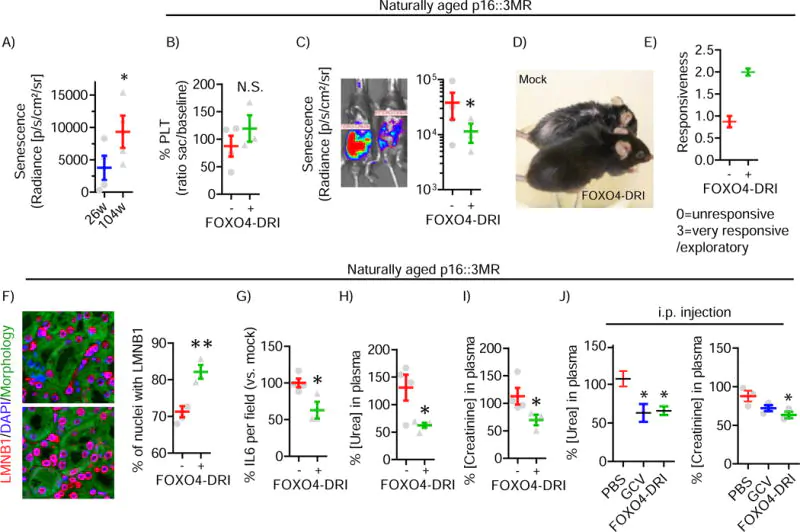
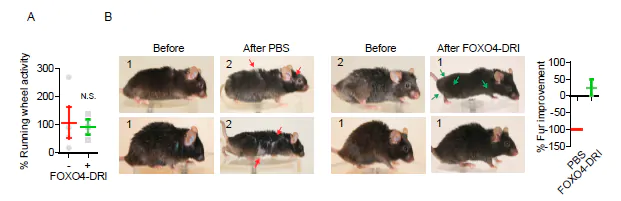
원천:PubMed.
Foxo 단백질은 인슐린 신호 전달의 중요한 조절제이지만 인슐린 유사 성장 인자뿐만 아니라 인슐린 자체의 하류에서 작용한다는 것이 오랫동안 이해되어왔다. 동물 모델에 대한 연구에 따르면 Foxo는 세포 대사, 성장, 분화, 산화 스트레스 등에 대한 인슐린 및 인슐린-유사 성장 인자의 억제제 효과를 매개한다는 것을 나타냅니다. FOXO의 돌연변이는 인슐린 신호 전달의 병리학 적 변화와 암뿐만 아니라 대사 질환의 발달과 관련이있다. 당뇨병 환자에서 FOXO 신호 전달의 변화는 공복 고혈당증 및 고지혈증으로 이어집니다.[6]. 후자는 신장 손상, 뇌졸중, 심장 마비, 상처 치유 장애 등과 같은 질병의 많은 합병증을 유발하기 때문에 당뇨병의 가장 관련이있는 부분 중 하나입니다. 당뇨병에서 FOXO 신호 전달을 조절하는 능력은 질병의 심각한 합병증을 예방하는보다 표적적이고 효과적인 방법을 제공 할 수 있습니다. FOXO4-DRI가 인슐린 신호 전달에 어떤 영향을 미치는지는 확실하지 않지만 단백질은 공복 혈당 수준을 감소시킴으로써 인슐린의 하류 효과를 향상시킬 수 있다고 생각됩니다.
나이는 심혈관 질환의 위험 인자입니다. 이 위험은 심장의 프로 테아 좀 활동 감소에 의해 매개되는 것으로 보인다. 프로 테아 좀은 세포가 "손상된"또는 기능 장애로 표시된 산화 된 단백질 및 기타 단백질을 제거 할 책임이있다. 쥐에 대한 연구는 나이가 프로 테아 좀 활동과 반비례 관계가있어 심장 내 손상된 단백질의 수준이 증가 함을 보여줍니다.[7].
Foxo 단백질은자가 포식 및 프로 테아 좀 활성을 매개합니다. FOXO4 수준의 증가는 프로 테아 좀 활성의 증가로 이어져 특정 조직 내에서 산화 및 단백질 손상 수준을 감소시켰다. Foxo4-Dri 또는 그 변형이 심장의 자연적인 하우스 키핑 기능을 향상시키고 심혈관 기능의 연령 관련 변화를 줄일 수 있습니다.[8].
인지 기능의 연령 관련 변화에는 복잡한 병인이 있습니다. 알츠하이머 병과 같은 비교적 흔한 질병조차도 의료계에서 완전히 이해되지 않습니다. 그러나 프로 테아 좀 활동의 변화가 기본 신경 퇴행성 조건으로 이어지거나 악화 될 수 있다는 개념을 뒷받침하는 몇 가지 증거가 있습니다. 프로 테아 좀 활동 장애가 알츠하이머 병과 같은 질병에 대한 주요 원인이거나 2 차 기여인지는 확실하지 않지만 Parkinson 's, Alzheimer's, Huntington 's 및 Prion Disease에서 시스템의 손상이 발견되었습니다. 근 위축성 측면 경화증 (ALS 또는 Lou Gehrig 's Disease에서 프로 테아 좀 기능의 손상이 있습니다.[9].
FOXO 단백질은 중추 신경계에서 변형 된 것으로 보이며, 연구원들은 외인성 FOXO 단백질이 신경 퇴행성 장애를 치료하거나 예방하는데 유용 할 수 있다는 생각을 탐구하게 된 것으로 보인다. 최소한 FOXO4-DRI 및 기타 변형 된 FOXO 단백질이 신경 퇴행성 장애의 끊임없는 진행을 늦추는 데 유용 할 수 있기를 희망합니다.[10].
FOXO4-DRI는 노화가 된 세포에서 아 pop 토 시스를 향상시켜 조직 기능이 향상되고 동물 모델에서 전반적인 건강을 향상시키는 것으로 명확하게 입증되었습니다. FOXO4-DRI의 영향이 얼마나 광범위한 지 볼 수는 있지만, 단백질이 치매, 심장병 및 세포 노화로 인한 일반적인 기능 상실과 같은 연령 관련 조건에 대한 통찰력을 발휘할 수 있기를 희망합니다.
FOXO4-DRI exhibits minimal side effects, low oral and excellent subcutaneous bioavailability in mice. Per kg dosage in mice does not scale to humans. FOXO4-DRI for sale at Peptide Gurus is limited to educational and scientific research only, not for human consumption. Only buy FOXO4-DRI if you are a licensed researcher.Peptidegurus는 미국에서 만든 연구 펩티드의 주요 공급 업체로 경쟁력있는 가격으로 최고 품질의 제품을 제공합니다. 우수성 및 고객 서비스에 중점을 두어 글로벌 배송으로 안전하고 편리한 주문 프로세스를 보장합니다.
© Copyright Peptide Gurus 2024. 모든 권리 보유.개인정보처리방침 이 사이트의 모든 제품은 연구, 개발용으로만 제공됩니다. 제품은 어떤 종류의 인간 섭취도 허용되지 않습니다. 이 웹사이트에 실린 진술들은 미국 식품의약국(FDA)이나 캐나다 보건부의 평가를 받은 적이 없습니다. 이 회사의 진술서와 제품은 어떠한 질병의 진단, 치료, 치유 또는 예방을 목적으로 하지 않습니다. 펩타이드구루스는 화학 공급업체입니다. 펩타이드구러스는 연방 식품, 의약품 및 화장품법 503A조에 정의된 조제 약국이나 화학 조제 시설이 아닙니다. 펩타이드 사이언스는 연방 식품, 의약품 및 화장품법 503B조에 따라 정의된 아웃소싱 시설이 아닙니다.
연락하다