유리 (1) 30 ml 세균성 물
자격을 갖춘 주문이 있습니다$ 500 USD.
(캡슐 제품, 미용 펩티드, 프로모션 코드 및 배송 제외)
LL-37은 모든 카텔 리시 딘과 마찬가지로 항균제, 항균, 항 바이러스, 항진균제를 가지며 염증을 감소시키는 것으로 나타났습니다. 연구에 따르면 특정 암에 대한 그 영향은 특정 환경에서 혈관 성장을 장려합니다.
제품 사용 :이 제품은 연구 화학 물질로만 의도 된 것입니다.이 명칭은 시험 관내 시험 및 실험실 실험에만 연구 화학 물질을 엄격하게 사용할 수있게한다. 이 웹 사이트에서 제공되는 모든 제품 정보는 교육 목적으로 만 사용됩니다. 인간이나 동물에 어떤 종류의 신체적으로 소개되는 것은 법에 의해 엄격히 금지되어 있습니다. 이 제품은 라이센스가 부여 된 자격을 갖춘 전문가 만 처리해야합니다. 이 제품은 약물, 음식 또는 화장품이 아니며 약물, 음식 또는 화장품으로 잘못 브랜드화되거나 잘못 사용되거나 오해가되지 않을 수 있습니다.
LL-37 (CAP-18)이란 무엇입니까?
LL-37은 유일하게 알려진 인간 카텔 리시 딘이며, 이는 다양한 기능을 가진 큰 단백질 패밀리입니다. 대 식세포 및 다형 핵 백혈구 (두 유형의 백혈구)에서 주로 발견되는이 펩티드는 박테리아를 죽이는 데 중요하지만 다른 극적인 영향을 미치는 것으로 밝혀졌습니다. 전체 클래스는 종종 항균성 펩티드 (AMP)라고합니다. LL-37은자가 면역 질환, 암 및 상처 치유에서 중요한 역할을하는 것으로 밝혀졌습니다.
LL-37 구조

LL-37 연구
LL-37 및 염증성 질환
LL-37은 주로 항균성 펩티드로 청구되지만 실제로 건선, 루푸스, 류마티스 관절염 및 죽상 동맥 경화증과 같은 다수의 염증성 질환에서 중요한 역할을합니다. 국소 염증 환경과 관련된 특정 세포에 따라 LL-37은 여러 가지 면역계 조절 행동을 가지고 있습니다. 그것은 다음과 같습니다.- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- IL-18 생산량을 늘리고
- 죽상 경화성 플라크의 수준을 감소시킵니다[1].
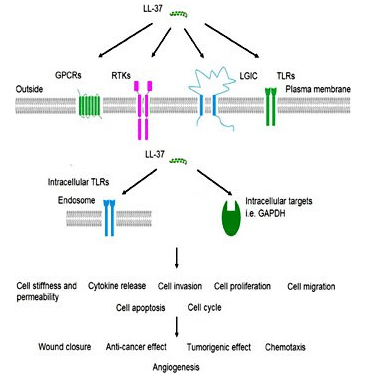
LL-37은 강력한 항균제입니다
LL-37은 선천성 면역계의 일부이며, 따라서 감염 동안 활성화되는 최초의 면역계 중 하나입니다. 피부 감염에 대한 연구에 따르면 정상 피부 수준은 LL-37 수준이 매우 낮지 만 펩티드는 침입 병원체의 존재하에 빠르게 축적된다는 것을 시사합니다. 펩티드는 감염과 싸우기 위해 인간 베타-디펜신 2와 같은 다른 단백질과 함께 작용하는 것으로 나타났습니다.[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 및 폐 질환
위에서 언급했듯이 LP는 박테리아 세포벽에 고유하지 않습니다. 그것은 다수의 다른 유기체에서 발견되며, 경우에 따라 환경이 곰팡이 나 다른 곰팡이에 의해 오염 될 때 공기가됩니다. LPS가 흡입되면, 정상 폐 조직은 생산에 의해 반응한다. 불행히도, 독성 먼지 증후군과 천식, COPD 등과 같은 호흡기 질환의 병인을 예방하기 위해 반응은 종종 부적절합니다. 독성 먼지 증후군에 대한 흡입 치료로서 LL-37의 사용에 대한 연구는 현재 진행 중입니다.[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].관절염에서 LL-37 이해
쥐에 대한 연구에 따르면 LL-37은 류마티스 관절염에 의해 영향을받는 관절의 고농도에서 발견됩니다. 특히, 펩티드는 관절염의 병리학 적 사건과 관련이있는 것으로 보인다. 그러나 펩티드가 원인 이거나이 관절의 상향 조절이 신체의 병리학 적 과정을 통제하려는 시도의 일부라면 분명하지 않습니다.[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. 이 연구에 근거하여, LL-37은 아마도 관절염에 보호 활성을 가지고 있다고 추측하는 것이 합리적이며, 이는 상당한 염증을 가진 조직에서 고농도를 설명 할 수 있습니다. 이 추측은 LL-37과 그 유도체가 염증성 관절염의 심각성과 직접 관련된 분자 인 Interleukin-32로 인한 염증을 조절하는 것으로 나타났습니다.[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. LL-37은 TLR4에 결합하고 전 염증성 또는 항 염증 효과를 촉진하는 것으로 나타났다. TLR3 상향 조절 설정에서 수행하는 것은 명확하지 않지만 연구가 진행 중입니다. LL-37이 과거에 전 염증성 대 식세포 반응을 선택적으로 감소시키는 것으로 밝혀 졌다는 점을 감안할 때 염증이 선택적으로 감소 할 수 있다는 생각은 불합리하지 않습니다.[13].LL-37 및 장
세포 배양에 대한 연구에 따르면 LL-37은 장에 몇 가지 효과가 있습니다. 먼저, 펩티드는 장의 상피 장벽을 유지하는 데 필요한 세포의 이동을 증가시킨다. 둘째, LL-37은 장 염증의 설정에서 아 pop 토 시스를 감소시켜 다수의 염증성 조건의 발병력을 늦추는 데 도움이된다. 전반적으로, 연구에 따르면 LL-37은 염증성 장 상태, 장 수술 후 또는 급성 장 감염의 설정에서 유용한 보조 치료법 일 수 있습니다. 항생제 요법의 보조제로 유용 할 수도 있으며, 종종 구강 항생제 사용을 제한하는 GI 부작용을 예방하는 데 도움이됩니다.[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. 현재, TNF- 알파 억제제는 염증성 장 상태에 대한 치료의 주류이다. 그들은 효과적인 약물이지만 결핵과 같은 심각한 감염의 위험이 급격히 증가하는 등 여러 가지 심각한 부작용이 있습니다. 염증성 장 질환의 LL-37 기반 치료의 발달은 TNF- 알파 억제제에 대한 의존도를 줄이고이 환자 집단에서 이환율 및 사망률을 향상시키는 데 도움이 될 수 있습니다.LL-37 및 장암
LL-37 및 암에 관한 연구는 혼합 결과를 일으켰지 만 펩티드는 흡연 및 담배 사용과 관련된 구강 편평 세포 암종을 포함하여 장 및 위암의 설정에 유리한 것으로 보인다. 흥미롭게도, 이러한 효과는 비타민 -D 의존 경로에 의해 매개되는 것으로 보이며, 왜 비타민을 복용하는 것이 이전에 GI 암에 대한 위험 감소와 관련이 있는지 설명 할 수 있습니다. 비타민 D는 LL-37을 통해 종양 관련 대 식세포의 항암 활성을 유도하는 것으로 보인다.[16].LL-37 및 혈관 성장
LL-37은 내피 세포에서 프로스타글란딘 E2 (PGE2)의 합성을 유발하는 것으로 보인다. PGE2는 염증성 통증 및 혈관의 성장과 관련이 있지만, 이러한 효과는 분자가 발현되는 위치에 따라 다릅니다. 내피 세포에서 PGE2는 혈관 신생이라는 과정에서 혈관의 발달을 유발합니다.[17]. 특정 설정에 따라 좋고 나쁘다. 혈관 신생을 조절하는 능력은 암 발달, 심장병, 뇌졸중 결과, 상처 치유 등에 영향을 미치기 때문에 지난 수십 년 동안 많은 연구의 초점이었습니다. LL-37 활성은 혈관 신생 경로를 조사하는 데 유용한 수단을 제공 할뿐만 아니라 필요할 때 혈관 성장을 촉진하고 (예 : 심장병)를 촉진하고 (예 : 암)를 낙담시키기위한 잠재적 인 미래 중재 모델을 제공합니다 (예 : 암).진행중인 LL-37 연구
LL-37의 흥미로운 점 중 하나는 다른 포유 동물과는 다른 구조가 있다는 것입니다.[18]. These alternative structures result in different functions for the same basic peptide and provide insight into how three-dimensional configuration can impact receptor binding. This feature makes LL-37 of intense interest because it allows scientists to study the impacts of simple amino acid sequence changes on structure and ultimately function. This could inform an entire branch of biochemistry and make it easier for scientists to manipulate protein production to achieve very specific results.
LL-37 exhibits minimal to moderate side effects, low oral and excellent subcutaneous bioavailability in mice. Per kg dosage in mice does not scale to humans. LL-37 for sale at
펩티드 전문가인간 소비가 아닌 교육 및 과학 연구로만 제한됩니다. 면허가있는 연구원 인 경우 LL-37 만 구매하십시오.
기사 저자
과학 저널 저자
Daniela Jindoli, PhD.트리 에스테 대학교 (University of Trieste), 유닛 · 생명 과학과에서 운영됩니다. 그녀의 초점은 그람 음성 박테리아, 전 염증 및 항 팽창 경로를 동시에 조절하는 것에 대한 LL-37의 생물학적 활성, LL-37의 항균 및 항균 효과를 둘러싸고있다.Daniela Jindoli, PhD.LL-37의 연구 및 개발에 관여하는 주요 과학자 중 한 명으로 언급되고 있습니다. 이 의사/과학자가 어떤 이유로 든이 제품의 구매, 판매 또는 사용을지지하거나 옹호하는 것은 아닙니다. 묵시적 또는 다른 방식으로 제휴 나 관계가 없습니다.
펩티드 전문가그리고이 의사. 의사를 인용하는 목적은이 펩티드를 연구하는 과학자들이 수행 한 철저한 연구 개발 노력을 인정, 인식 및 인정하는 것입니다. Daniela Xhindoli, PhD. 참조 인용에 따라 [18]에 나열되어 있습니다.
참조 인용
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.